美国食品药物管理局有史以来第一次通过以生物标志来做癌症治疗,因此加速通过了Keytruda® (pembrolizumab,默克药厂),来治疗成人与儿童的无法切除之肿瘤,例如MSI-H与dMMR,肿瘤在治疗后又成长或是没有其他适当的治疗方法。
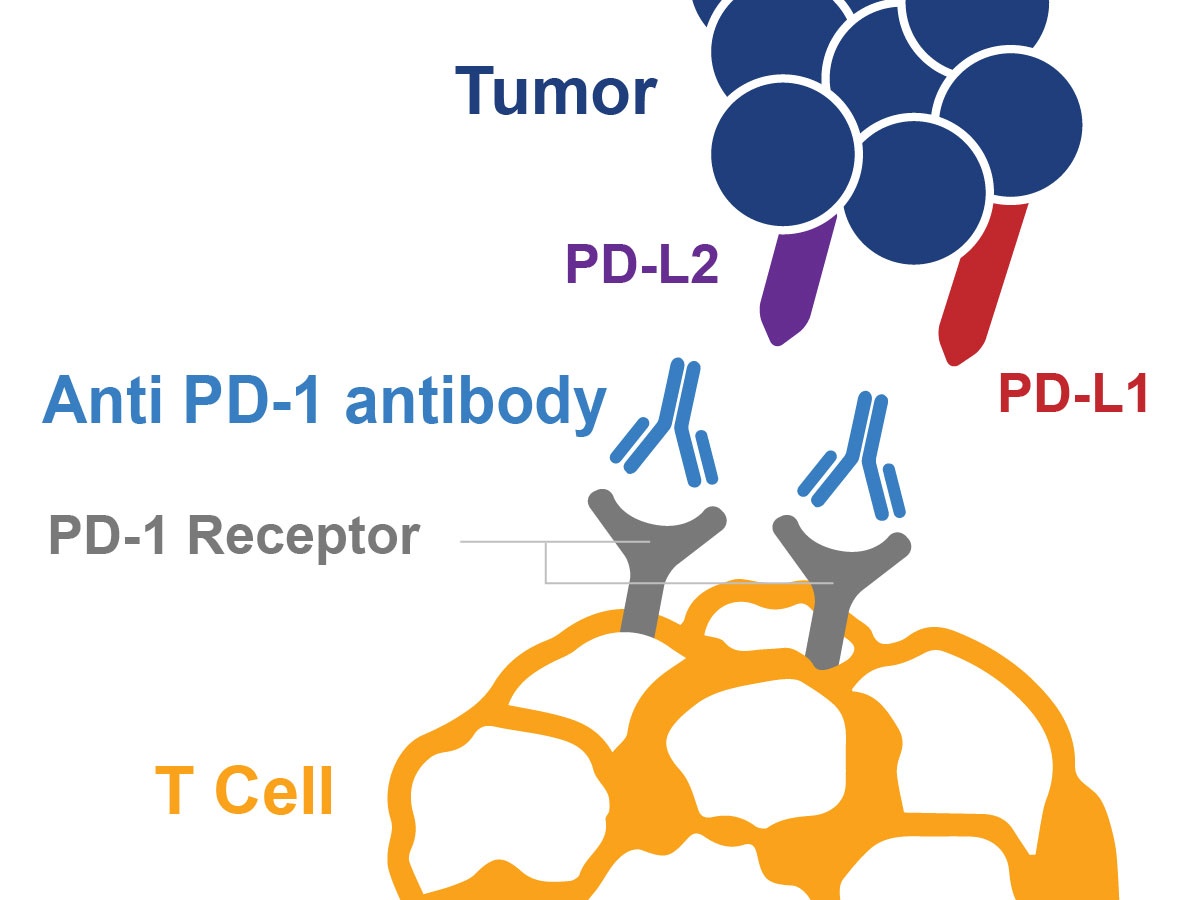
Keytruda是一设定好的PD-1阻断抗体, 能够帮助免疫系统阻挡肿瘤的回避机制。这项抗体已经通过认证,能够用来治疗很多种类的癌症像是黑色素瘤、非小细胞肺癌、头颈癌、泌尿上皮癌、以及霍奇金淋巴瘤。
新认证的DNA修复缺陷
MSI-H与dMMR的肿瘤让细胞失去了自我修复DNA的能力,因此让有DNA缺陷的细胞增生为癌症。但是一个病患若有较高的MSI-H或是dMMR突变负荷,则会被认为有较高频率的表位和免疫原性。高抗原负荷肿瘤则比较容易受到像是PD-1和PD-L1免疫检查点抑制剂的影响。
MSI-H与dMMR细胞可以在结肠直肠癌与胃癌的病患身上发现,所以此次通过认证将能够帮助到许多病患族群,因为有将近5%的转移性结肠直肠癌病患有MSI-H或是dMMR肿瘤。
第一/第二阶段研究帮助加速通过认证
这项认证是经过5项开放标签、在第一/第二阶段临床实验的149位,以15种MSI-H或dMMR归类出的肿瘤类型并接受Keytruda的病患来做为标準。其中有39.6%的病患有完整或是部分反应,在这些患者之中,则有78%的反应持续了至少六个月。
美国食品药物管理局药物研发中心肿瘤产品部Richard Pazdur说道「美国食品药物管理局目前为止已经通过认证的癌症疗法都是依据发源的位置来决定,例如肺癌或乳癌。我们现在则通过认证肿瘤生物标志的用药。」
个人化精準医疗将迈向实现的道路
这项根据生物标志而通过验证药物将是实现个人化精準医疗的一大关键,遗传性生物标志将能够用来决定治疗的发法,而不是单单找出癌症类型而已。
更多阅读在Nature News